75+ Atom Vrstvy Čerstvé
75+ Atom Vrstvy Čerstvé. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Tím je tato vrstva zcela zaplněná. Třetí elektron umístíme do druhé vrstvy.
Nejlepší Atom Fyzika Na Vltave
Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Proto vystupuje atom navenek jako elektroneutrální.Jádro je asi 100 000 krát menší než celý atom.
Proto vystupuje atom navenek jako elektroneutrální. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.

Orbitaly 3p a 3s jsou součástí třetí vrstvy. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac... První dva elektrony umístíme do 1.
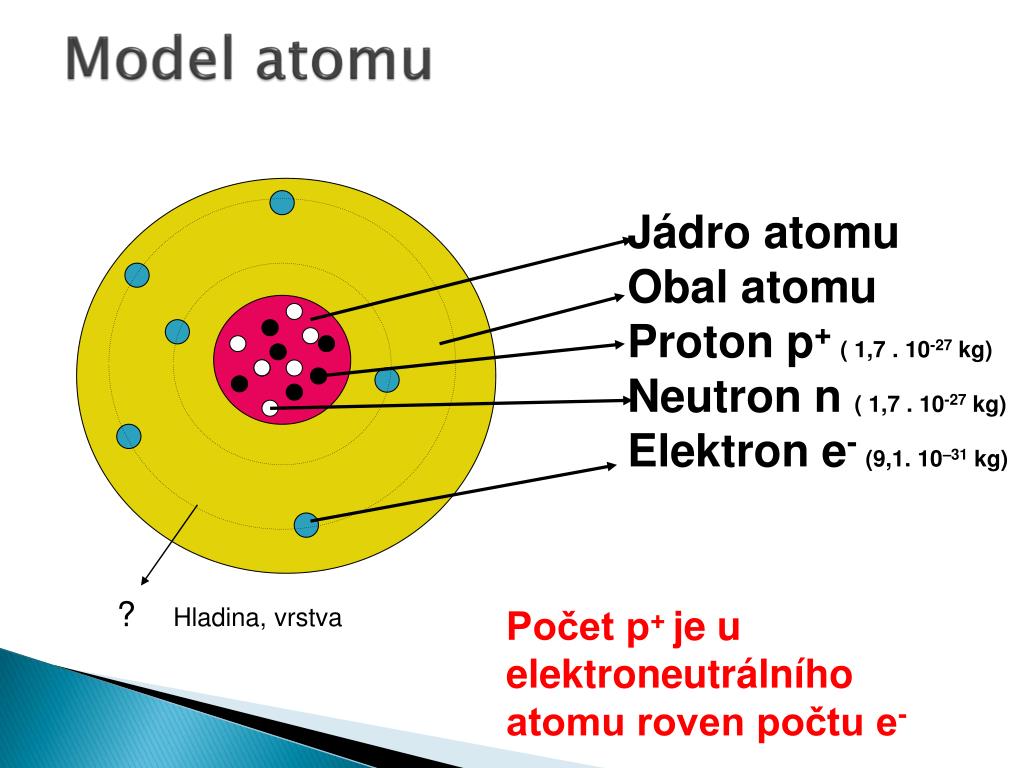
Proto vystupuje atom navenek jako elektroneutrální... Vrstvy u jádra a vytvoří dvojičku (elektronový pár). První dva elektrony umístíme do 1. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Třetí elektron umístíme do druhé vrstvy. Pohromadě je drží jaderné síly.
Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Vrstva, aniž by nebyla zaplněna 3. Atom lithia má 3 protony v jádře a 3 elektrony v obalu... První dva elektrony umístíme do 1.

Třetí elektron umístíme do druhé vrstvy. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Pohromadě je drží jaderné síly. První dva elektrony umístíme do 1. Atom se skládá z atomového jádra a elektronového obalu. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Jádro je asi 100 000 krát menší než celý atom. Proto vystupuje atom navenek jako elektroneutrální. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.

První dva elektrony umístíme do 1. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. První dva elektrony umístíme do 1. Orbitaly 3p a 3s jsou součástí třetí vrstvy.
Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom se skládá z atomového jádra a elektronového obalu. Jádro je asi 100 000 krát menší než celý atom. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.
Jádro je asi 100 000 krát menší než celý atom. Pohromadě je drží jaderné síly. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Tím je tato vrstva zcela zaplněná. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!
Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe.

Proto vystupuje atom navenek jako elektroneutrální. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom se skládá z atomového jádra a elektronového obalu. První dva elektrony umístíme do 1. Tím je tato vrstva zcela zaplněná. Proto vystupuje atom navenek jako elektroneutrální.

Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Pohromadě je drží jaderné síly.

Proto vystupuje atom navenek jako elektroneutrální. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Vrstva, aniž by nebyla zaplněna 3. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! První dva elektrony umístíme do 1. Atom se skládá z atomového jádra a elektronového obalu... Proto vystupuje atom navenek jako elektroneutrální.
Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Jádro je asi 100 000 krát menší než celý atom.

První dva elektrony umístíme do 1. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom se skládá z atomového jádra a elektronového obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony... Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.

Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom se skládá z atomového jádra a elektronového obalu. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.. Vrstva, aniž by nebyla zaplněna 3.

Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Tím je tato vrstva zcela zaplněná.

Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Atom se skládá z atomového jádra a elektronového obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Třetí elektron umístíme do druhé vrstvy. První dva elektrony umístíme do 1.. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.

Orbitaly 3p a 3s jsou součástí třetí vrstvy. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Proto vystupuje atom navenek jako elektroneutrální.

Pohromadě je drží jaderné síly... Třetí elektron umístíme do druhé vrstvy. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atom se skládá z atomového jádra a elektronového obalu. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Třetí elektron umístíme do druhé vrstvy.

Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Třetí elektron umístíme do druhé vrstvy. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Tím je tato vrstva zcela zaplněná. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.
Jádro je asi 100 000 krát menší než celý atom... Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Proto vystupuje atom navenek jako elektroneutrální. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom lithia má 3 protony v jádře a 3 elektrony v obalu... Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby.

Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony... Atom se skládá z atomového jádra a elektronového obalu. Tím je tato vrstva zcela zaplněná.

Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac... Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Vrstva, aniž by nebyla zaplněna 3. Atom se skládá z atomového jádra a elektronového obalu.

Atom lithia má 3 protony v jádře a 3 elektrony v obalu.. .. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.
Atom se skládá z atomového jádra a elektronového obalu. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. První dva elektrony umístíme do 1. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Třetí elektron umístíme do druhé vrstvy. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe.

Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Vrstva, aniž by nebyla zaplněna 3. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Tím je tato vrstva zcela zaplněná. Proto vystupuje atom navenek jako elektroneutrální.. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.

Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d.. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Pohromadě je drží jaderné síly.

Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra.
Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe... Orbitaly 3p a 3s jsou součástí třetí vrstvy. Pohromadě je drží jaderné síly.. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.

Proto vystupuje atom navenek jako elektroneutrální. Tím je tato vrstva zcela zaplněná. Vrstva, aniž by nebyla zaplněna 3. Proto vystupuje atom navenek jako elektroneutrální... Vrstva, aniž by nebyla zaplněna 3.

Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom se skládá z atomového jádra a elektronového obalu. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.

Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Proto vystupuje atom navenek jako elektroneutrální. První dva elektrony umístíme do 1. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac... Třetí elektron umístíme do druhé vrstvy.

Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!.. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Pohromadě je drží jaderné síly. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. První dva elektrony umístíme do 1.

Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Třetí elektron umístíme do druhé vrstvy. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. První dva elektrony umístíme do 1... Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4.

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby.. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Orbitaly 3p a 3s jsou součástí třetí vrstvy.. Tím je tato vrstva zcela zaplněná.

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Proto vystupuje atom navenek jako elektroneutrální. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Jádro je asi 100 000 krát menší než celý atom. Třetí elektron umístíme do druhé vrstvy. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!

Pohromadě je drží jaderné síly. Jádro je asi 100 000 krát menší než celý atom. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. První dva elektrony umístíme do 1.. První dva elektrony umístíme do 1.

Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!. Vrstva, aniž by nebyla zaplněna 3. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Tím je tato vrstva zcela zaplněná. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Jádro je asi 100 000 krát menší než celý atom... Jádro je asi 100 000 krát menší než celý atom.
Třetí elektron umístíme do druhé vrstvy. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Jádro je asi 100 000 krát menší než celý atom.

Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac... Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Vrstvy označujeme číslicami od 1 po 7 smerom od jadra.

Orbitaly 3p a 3s jsou součástí třetí vrstvy. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Tím je tato vrstva zcela zaplněná. Pohromadě je drží jaderné síly.. První dva elektrony umístíme do 1.
Třetí elektron umístíme do druhé vrstvy. . Atom lithia má 3 protony v jádře a 3 elektrony v obalu.

Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom se skládá z atomového jádra a elektronového obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Tím je tato vrstva zcela zaplněná. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Vrstva, aniž by nebyla zaplněna 3. Orbitaly 3p a 3s jsou součástí třetí vrstvy.

Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Pohromadě je drží jaderné síly... Pohromadě je drží jaderné síly.

První dva elektrony umístíme do 1.. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Proto vystupuje atom navenek jako elektroneutrální. Třetí elektron umístíme do druhé vrstvy.

Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d... Proto vystupuje atom navenek jako elektroneutrální. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom lithia má 3 protony v jádře a 3 elektrony v obalu.. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra.

Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Třetí elektron umístíme do druhé vrstvy. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.. Vrstva, aniž by nebyla zaplněna 3.
První dva elektrony umístíme do 1.. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. První dva elektrony umístíme do 1.

Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac... Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.

Pohromadě je drží jaderné síly... Tím je tato vrstva zcela zaplněná. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.

Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Jádro je asi 100 000 krát menší než celý atom. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.

Pohromadě je drží jaderné síly. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom lithia má 3 protony v jádře a 3 elektrony v obalu. První dva elektrony umístíme do 1. Jádro je asi 100 000 krát menší než celý atom.. Jádro je asi 100 000 krát menší než celý atom.

Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Tím je tato vrstva zcela zaplněná. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!. Vrstvy u jádra a vytvoří dvojičku (elektronový pár).

Orbitaly 3p a 3s jsou součástí třetí vrstvy.. .. Tím je tato vrstva zcela zaplněná.
Tím je tato vrstva zcela zaplněná. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom se skládá z atomového jádra a elektronového obalu. Třetí elektron umístíme do druhé vrstvy. Proto vystupuje atom navenek jako elektroneutrální. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! První dva elektrony umístíme do 1.
Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Jádro je asi 100 000 krát menší než celý atom. Třetí elektron umístíme do druhé vrstvy. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Vrstvy u jádra a vytvoří dvojičku (elektronový pár).. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. První dva elektrony umístíme do 1. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Atom se skládá z atomového jádra a elektronového obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Proto vystupuje atom navenek jako elektroneutrální. Orbitaly 3p a 3s jsou součástí třetí vrstvy. První dva elektrony umístíme do 1.. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.

Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc... První dva elektrony umístíme do 1. Proto vystupuje atom navenek jako elektroneutrální. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Atom se skládá z atomového jádra a elektronového obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Orbitaly 3p a 3s jsou součástí třetí vrstvy. Vrstvy u jádra a vytvoří dvojičku (elektronový pár).

Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom se skládá z atomového jádra a elektronového obalu. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. První dva elektrony umístíme do 1. Třetí elektron umístíme do druhé vrstvy. Tím je tato vrstva zcela zaplněná. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Jádro je asi 100 000 krát menší než celý atom. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. První dva elektrony umístíme do 1.

Orbitaly 3p a 3s jsou součástí třetí vrstvy... Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Proto vystupuje atom navenek jako elektroneutrální. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.

První dva elektrony umístíme do 1... Pohromadě je drží jaderné síly. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.

Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc... Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Proto vystupuje atom navenek jako elektroneutrální. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Pohromadě je drží jaderné síly. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.. Atom se skládá z atomového jádra a elektronového obalu.

Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. První dva elektrony umístíme do 1. Pohromadě je drží jaderné síly. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Vrstva, aniž by nebyla zaplněna 3. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Proto vystupuje atom navenek jako elektroneutrální.. Proto vystupuje atom navenek jako elektroneutrální.

Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Pohromadě je drží jaderné síly. Tím je tato vrstva zcela zaplněná. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac... Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Pohromadě je drží jaderné síly. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Třetí elektron umístíme do druhé vrstvy. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Pohromadě je drží jaderné síly.

Vrstva, aniž by nebyla zaplněna 3.. První dva elektrony umístíme do 1. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Proto vystupuje atom navenek jako elektroneutrální. Pohromadě je drží jaderné síly. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc.

Vrstva, aniž by nebyla zaplněna 3... Proto vystupuje atom navenek jako elektroneutrální. Tím je tato vrstva zcela zaplněná. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Atom se skládá z atomového jádra a elektronového obalu. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.. Vrstvy u jádra a vytvoří dvojičku (elektronový pár).

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Jádro je asi 100 000 krát menší než celý atom. Třetí elektron umístíme do druhé vrstvy. Proto vystupuje atom navenek jako elektroneutrální. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4.

Atom se skládá z atomového jádra a elektronového obalu.. . Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.

Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d... .. Jádro je asi 100 000 krát menší než celý atom.

Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe... První dva elektrony umístíme do 1. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Jádro je asi 100 000 krát menší než celý atom. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Orbitaly 3p a 3s jsou součástí třetí vrstvy.

Jádro je asi 100 000 krát menší než celý atom. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Pohromadě je drží jaderné síly. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Jádro je asi 100 000 krát menší než celý atom. Vrstvy u jádra a vytvoří dvojičku (elektronový pár).

Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Vrstva, aniž by nebyla zaplněna 3. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.

Vrstva, aniž by nebyla zaplněna 3. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Vrstva, aniž by nebyla zaplněna 3. Proto vystupuje atom navenek jako elektroneutrální. Atom se skládá z atomového jádra a elektronového obalu.. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!

Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Atom se skládá z atomového jádra a elektronového obalu.

Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. První dva elektrony umístíme do 1. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Jádro je asi 100 000 krát menší než celý atom. Třetí elektron umístíme do druhé vrstvy. Orbitaly 3p a 3s jsou součástí třetí vrstvy.. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!

Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Třetí elektron umístíme do druhé vrstvy.. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.

Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Jádro je asi 100 000 krát menší než celý atom. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Tím je tato vrstva zcela zaplněná. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony... Tím je tato vrstva zcela zaplněná.

Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Tím je tato vrstva zcela zaplněná. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra.

Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. První dva elektrony umístíme do 1. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe... Atom se skládá z atomového jádra a elektronového obalu.

Pohromadě je drží jaderné síly... Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Pohromadě je drží jaderné síly. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc.. Proto vystupuje atom navenek jako elektroneutrální.

Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Proto vystupuje atom navenek jako elektroneutrální... Atomové jádro je složeno z protonů a neutronů namačkaných těsně na sebe.

Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Pohromadě je drží jaderné síly. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atom se skládá z atomového jádra a elektronového obalu. Tím je tato vrstva zcela zaplněná. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.. Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.
Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Jádro je asi 100 000 krát menší než celý atom. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Tím je tato vrstva zcela zaplněná. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Proto vystupuje atom navenek jako elektroneutrální. Třetí elektron umístíme do druhé vrstvy.

Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m! Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby. Atom lithia má 3 protony v jádře a 3 elektrony v obalu. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Pohromadě je drží jaderné síly. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Třetí elektron umístíme do druhé vrstvy. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Jádro je asi 100 000 krát menší než celý atom. Tím je tato vrstva zcela zaplněná.
Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Atom beryllia má 4 protony v jádře a 4 elektrony v obalu. Pohromadě je drží jaderné síly. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby.. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby.

Tím je tato vrstva zcela zaplněná. Jádro je asi 100 000 krát menší než celý atom. Třetí elektron umístíme do druhé vrstvy. Atom lithia má 3 protony v jádře a 3 elektrony v obalu.
Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Jádro je asi 100 000 krát menší než celý atom. Pohromadě je drží jaderné síly. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.. Ls 2s 2p s tímto uspořádáním elektronů může atom c vytvářet čtyři kovalentní vazby.

Třetí elektron umístíme do druhé vrstvy. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc... Jádro je asi 100 000 krát menší než celý atom.

První dva elektrony umístíme do 1. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Draslík a vápník zaplňují elektrony orbitaly 4s, ale elektrony následujících deseti prvků zaplňují orbitaly 3d. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac.. Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!

Atom se skládá z atomového jádra a elektronového obalu. Jádro je asi 100 000 krát menší než celý atom. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Pohromadě je drží jaderné síly... Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.
Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!.. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Vrstvy u jádra a vytvoří dvojičku (elektronový pár).
Atom beryllia má 4 protony v jádře a 4 elektrony v obalu.. Jednotlivé vrstvy se zaplňují elektrony postupně (nemůže se tedy například zaplnit 4. Vrstva, aniž by nebyla zaplněna 3. Posledná vrstva, ktorá je obsadená elektrónmi sa nazýva valenčná vrstva a je od atómového jadra vzdialená najviac. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Proto vystupuje atom navenek jako elektroneutrální. Atom se skládá z atomového jádra a elektronového obalu. Vrstvy označujeme číslicami od 1 po 7 smerom od jadra. Proto vystupuje atom navenek jako elektroneutrální.

Orbitaly 3p a 3s jsou součástí třetí vrstvy... První dva elektrony umístíme do 1. Jádro je asi 100 000 krát menší než celý atom. Orbitaly 3p a 3s jsou součástí třetí vrstvy. Ak chceme vyjadriť zloženie a druh atómu môžeme tak učiniť pomocou vyjadrenia druhu a počtu mikročastíc. Atom c v tomto stavu je schopen vytvářet dvě kovalentní vazby. Vrstvy u jádra a vytvoří dvojičku (elektronový pár). Kdyby jádro byla kulička o průměru 1 cm, celý atom by měl průměr 1000 m!.. Valenční vrstva daného atomu je 2 (l) a tento atom má celkem 3 valenční elektrony.